L13 水的硬度
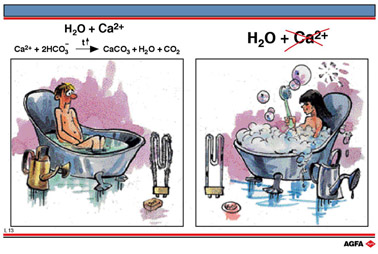
目标:表明了硬水可以使肥皂生成浮渣以及它阻碍了水的沸腾。 |
有两种类型的硬水:由于碳酸氢钙Ca(HCO3)2
溶解于水形成的暂时硬水,以及钙离子和镁离子的硫酸盐溶解于水形成的永久硬水。暂时硬度能够通过煮沸而除去,而永久硬度则不能。
所以硬水可以包含钙离子 (Ca2+)或镁离子(Mg2+)或者两者都有。自来水的硬度等级主要在于水中的钙离子浓度。

当包含在暂时硬水中的碳酸氢钙受热时发生分解:
![]()
得到了一种不溶性的沉淀——碳酸钙(CaCO3)。这种沉淀作用发生在受热的锅炉和水壶中。而当这中沉淀越来越厚的时候,则加热水需要更多的热量。
水的硬度可以通过很多方式表示。为了解释方便,我们假设硬度都是由钙离子引起的。
- 以钙离子的物质的量浓度表示。
- 以ppm的CaCO3表示。
(1ppm CaCO3 =1mg CaCO3/ kg water = 0.01mmol Ca2+ ions /L.)
在英国,水的硬度与水源有关,例如来自苏格兰花岗岩山上的水是软的,而来自奔宁山脉的石灰石山上的水是硬的。
虽然硬水对于饮用并无害处,但是它使热水管和锅炉结垢,并且增加了肥皂的消耗量。