L03 酸雨
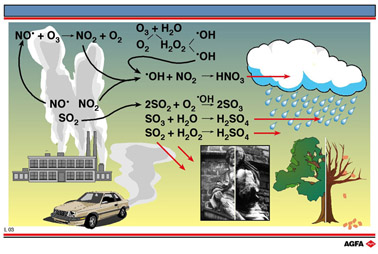
目标:说明酸雨如何产生及它造成的后果。 |
在内燃机里,高温条件使氮与氧发生了反应,这就是工业和交通释放出氮的氧化物(NOx) 的原因。而当火山爆发或者含硫燃料(例如煤)燃烧的时候,二氧化硫和三氧化硫就进入了大气层。这些气体可以通过多种方式蓄积,可能以酸性气体或者酸性微粒的形式被风带到距离污染源几百公里以外,也可能溶于雨或雪形成酸, 也就形成了所谓的“酸雨”。无论哪种形式的蓄积,对环境同样都是有害的。
纯水包含有同等数目的H3O+(水合 H+)和 OH-; 因此纯水的ph是7。由于每升空气中存在 350 微升的CO2, 所以自然界的雨水通常显示弱酸性。
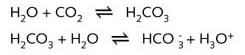
其pH在4.9和6.5之间。酸雨比自然雨水有更高的酸度(更低的pH)。
当一氧化氮自由基(NO·)在大气层中产生的时候,它会迅速转变为NO2。进一步与氢氧自由基(HO·) 反应生成硝酸。

当二氧化硫( (SO2) 进入空气中的时候,它很容易被氧气O2 (+HO•)或者过氧化氢 H2O2 (见图示“光化学烟雾”)。
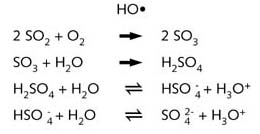
正是这些反应的结果,雨水的pH下降到3与4之间,也即酸度增强了。这个pH已经接近乙酸溶液了。 据测定,洛杉矶酸雾的pH竟低达1.7。
酸雨已经对环境产生了多种严重的影响。过高的酸度大大超越了土壤的缓冲能力。 某些地区的土壤缓冲能力不足,难以抵消雨水的酸度,所以地表水酸度迅速增加(已经发现北欧的湖泊酸度很强)。像鱼卵这种很敏感的生物体在这种环境中将不能够存活。
如果土地的pH降到3的话,原本对于植物健康成长有利的微量元素将对植物产生毒性,例如黏土释放出的钙、镁和铝离子。庄稼,甚至包括树木,都将因为基本养分的匮乏和铝离子中毒而死亡。在加拿大、 挪威、瑞典、威尔士和苏格兰等地区的湖泊中,高浓度的铝离子杀死了很多鱼类。铝离子干扰了鱼类的鳃,使它们被一些黏液阻塞,因为呼吸不到足够的氧气而无法生存。 对于树叶和树木的破坏也不能完全归罪于酸雨。臭氧浓度的增加与疾病的蔓延和泛滥也扮演了很重要的角色。
酸雨对于用石灰石、大理石和沙岩(被碳酸钙或者氧化铁包裹的石英颗粒)建造的建筑物破坏尤为明显。原因在于碳酸钙被溶解为碳酸氢钙和硫酸钙而流失。这就形成了我们熟悉的岩石表面的损耗现象。
![]()
硅酸盐成分的岩石受高酸度的影响则较弱。