R01 - R02 非氧化还原与氧化还原反应
目标:说明某些化学反应涉及电学性质, |
化学反应可以分为多种类型,在此列举几类:化合反应、分解反应、复分解反应、置换反应、沉淀反应、 酸碱反应和氧化还原反应。
以上反应类型中,有些涉及(带电)原子电子构型的变化,有些则不然,例如:(i) 离子化合物能在水中解离为具有自身组分的离子;(ii)离子在溶液中可以形成晶状的沉淀等。但是,它们都是化学反应。
非氧化还原反应
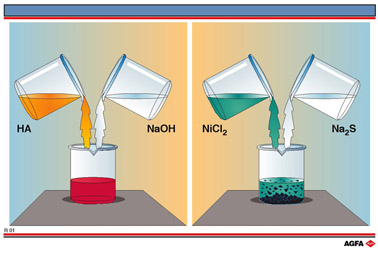
图R01描述了解释两类化学反应的简单实验,其中,(带电)原子的电子构型都没有改变。
R01左边部分表示的是无色氢氧化钠(NaOH)水溶液加到弱酸性水溶液中,后者含有酚红指示剂,因而呈黄色。酚红是一种在水中可解离的弱酸:
![]()
如果向溶液中加酸,反应会向左进行形成黄色的HA。如果向溶液中加碱,例如氢氧化钠,反应会向 右进行形成红色的A-。
![]()
这类酸碱反应称为质子转移反应。OH-从HA中夺走一个质子。
R01右边部分表示的是绿色氯化镍(NiCl2)水溶液与无色硫化钠水溶液反应。当两种溶液混合后,可观察到颜色发生变化,这是不能用物理稀释来解释的。原先绿色的氯化镍溶液颜色变浅,里面还分布着黑色的沉淀物,该黑色沉淀是硫化镍(NiS)。
当两种盐(氯化镍和硫化钠)在水中溶解时,它们发生电离:
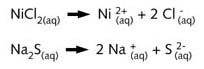
镍离子(Ni2+)与硫离子(S2-)反应,生成硫化镍(NiS)晶体,产生沉淀。
这类化学反应称为沉淀反应。并非所有有色溶液与无色溶液的混合后都发生质子转移或沉淀反应。
氧化还原反应
图R02左边描述了一个简单的化学实验,在这个反应中,(带电)原子的电子构型发生了改变。无色碘化钾(KI)水溶液与黄色氯化铁(FeCl3)水溶液混合,生成红棕色的溶液。这两种盐在水中电离:
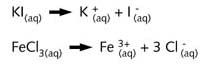
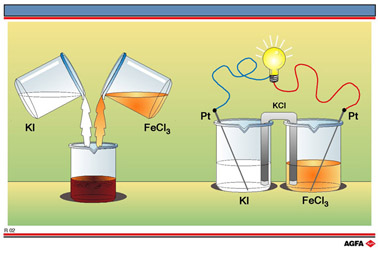
由于在这个反应中既无质子转移也无沉淀生成,所以它肯定属于另一种反应类型。它的反应类型可以用另一种方式证明,例如R02右图所示,用同样的试剂在不同条件下进行反应。
在此,两个试剂没有像左图那样混合,而是改用一种叫做盐桥的装置连接起来。这种装置不让两份溶液混合,但允许阳离子(带正电荷的离子)和阴离子(带负电荷的离子)移动。所用盐桥为一个U形管,里面装填含有电解质氯化钾(KCl)的琼脂凝胶。
在两个溶液中分别插入惰性的铂棒,它们又用金属线连接在一个小功率的灯泡上。另一种实验是用安培计或伏特计取代这个灯泡,这样可以检测到微弱的电流。把铂金属棒换成表面积大的铂箔片可以增大电流。灯泡闪亮说明回路中有电流流过,也就 是说,在两种化学试剂之间有电子在转移。
这种反应称为电子转移反应。这种反应只能在溶液不能直接混合的装置上才能得到证明。如果将电极都放在R02左图所示的大烧杯底上,会发现电极间没有电流通过。这并不意味着碘化钾和氯化铁直接反应时没有发生电子转移,它只是说明电子不经电极转移,而是从碘离子直接传递给了三价铁离子。这可表示为:
![]()
反应本身可表示为两个半反应方程式:
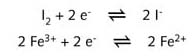
碘离子(I-)失去的电子全部传递给了铁离子(Fe3+)。在左边的装置中,发生的是直接电子转移反应,水中没有电子流出。电子直接从一个粒子(分子或离子)转移到另一个粒子(分子或离子)。在R02右边所示的装置中,电子由I-通过导线传递给Fe3+,并经过灯丝,传递速率比上一情况慢得多。不同的电荷载体——离子(阴离子或阳离子)——使电荷可以通过盐桥传递,以及可以在溶液中传递。图R03给出了具体细节。
此外,盐桥确保两种溶液不相互扩散。
这个小探索揭示了的确存在这样一种独特而又十分有趣的化学反应。然而,你可能会想到,是否所有 化学反应都可归结到这一类型?因此,绝对有必要对其他反应(例如R01所列反应)进行验证。用一个与 图 R02(右边)类似的装置检验质子转移反应(R01 左图)和沉淀反应(R01 右图),发现不存在电流。