R13 抗腐蚀:表面处理
目标:阐明抗腐蚀所用表面处理方法的优点与缺点。 |
人们发明了各种抗腐蚀的方法,这些方法涉及到以下因素:
1.
阳极表面或阳极半反应;
2.
阴极表面;
3.
电解;
4.
氧化剂的性质;
5.
电子的传递能力。
例如,在金属表面涂一薄层油漆(涂漆),镀一层金属锌(镀锌)或镀一层金属锡(镀锡),覆盖在金属表面上,这些方法可以改变阳极表面性质,从而保护金属免遭腐蚀。
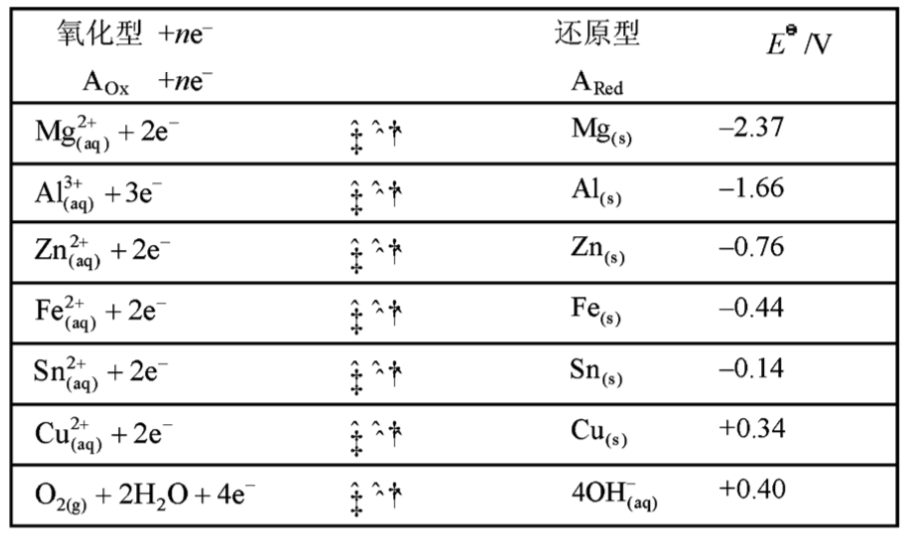
图R12和R13所需半反应的标准电极电势为:
如果给铁镀上一层0.1~0.5 mm厚的锌,由于下述两个原因,铁受到保护:
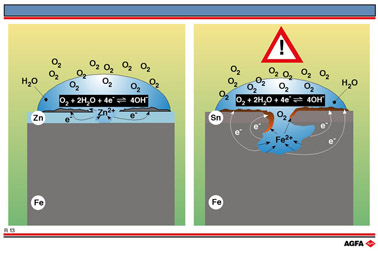
由于Zn2+/Zn电对的电极电势值更负,这就确保在腐蚀过程中首先被腐蚀的是锌,而不是铁。此外,即使锌镀层上存在一些细小缺损,由于在表面存在电化学电池,在电池中是还原性强的Zn2+/Zn电对作阳极,Fe3+/Fe电对作阴极,所以仍然是锌首先被氧化腐蚀,保护了下面的铁免遭腐蚀。尽管锌镀层很薄,但保护作用可维持很长时间。
在食品工业中,常用极薄的锡镀层来保护罐头的铁皮。由于Fe2+/Fe电对的标准电极电势位于Sn2+/Sn电对的上方,说明铁氧化腐蚀比锡容易,如图R13的右侧所示。如果罐头的锡镀层被剐破,铁皮将遭腐蚀。 由于罐头的镀锡层破损后将发生局部的严重腐蚀,罐头的里面如果已经锈蚀,锡离子有可能进入食品中,虽然其毒性不太大,但应该避免食用这种罐头食品。显然罐头镀锡有这些缺点,但仍广泛应用于食品工业中,毕竟罐头内部被剐破的机会是很小的,所以它仍不失为一种保护铁的好办法。