R18 - R19 氯碱工业生产氯气:汞电解槽、隔膜电解槽与薄膜电解槽
目标:图解描述世界范围内电解生产两种最重要基础化工产品 NaOH 和 Cl2 的工艺过程。 |
氯碱工业是化学工业的一个重要分支,通过电解普通食盐生产氯气和氢氧化钠。主要原料为盐水——氯化钠(NaCl)饱和水溶 液,源自天然食盐。Cl2 的年产量为 5000 万吨。其部分市场份额用于饮用水消毒和游泳池消毒,大多数则用于(聚)氯乙烯和其他含 氯碳氢化合物的合成工业,例如生产氯代烷烃溶剂、制冷剂、消毒液、农药和杀真菌剂等等。电解生产氯气的同时,得到两种有用的副产物——氢氧化钠和氢气。以下半反应有助于深入了解这一工艺过程:
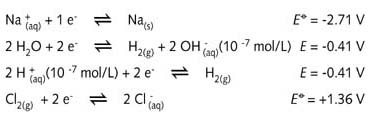
按中性水的H+ 和 OH- 的浓度计算,
E 为 -0.41 V.
理论上,由于在标准电极电势表中,这三种物质都位于Cl的左上方,因此Cl- 与Na+、 H+或H2O分子反应都可以生产氯气。但是这些反应都是不能自持的。要让反应进行需要持续提供电能,即需要电解工艺过程。在理论上,Cl-电解还原Na+的过程不仅能产生Cl,而且还能产生钠固体Na(s)。但是,金属钠会立即与电解槽里的水和/或H+反应,生成氢气和OH-(即NaOH溶液)。
这一工艺十分有用,因为单个工艺能同时生产三种重要的化工产品。但是,有一个问题。由于氯气在氢氧化钠碱性溶液中生成,两者会结合形成ClO-与Cl-。结果产生家用漂白粉的一种组分:次氯酸钠 NaClO。为解决这一问题,必须在氯气和氢氧化钠相遇反应之前,就把它们从电解池里取出来。
目前有三种工业电解工艺用来生产氯气,它们都已克服了上面提到的问题。
1. 汞电解槽
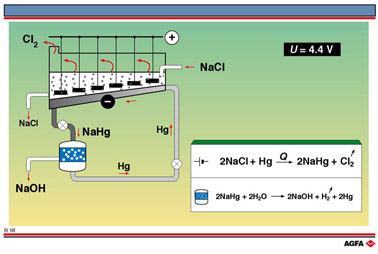
R18图示的这种电解槽用于生产氯气和氢氧化钠,使用食盐饱和溶液,工作电压为4.4 V。电解食盐溶液通常在阴极产生氢气,但如果用汞作阴极材料,就不会出现这种情况。在带负电的汞阴极上,氢有很高的过电势,意味着需要更高的负电压,氢离子才能放电。与此同时,钠原子与汞结合生成汞齐,因此Na+的放电电压降低。这也阻止了钠与水接触发生反应,避免了碱性介质的问题。
氯气在带正电的阳极上生成,阳极过去是一串悬挂的石墨棒,现在正用更贵但也更耐用的钛或铂-合金钢替代。在电解槽顶部收集生成的氯气。
钠汞齐在电解槽底部流走,进入含有石墨球的分离槽。石墨催化自持的钠汞齐解离反应。解离出来的钠与水反应,形成氢氧化钠和氢气。再生的汞又回到电解槽中。
![]()
电解槽消耗的盐水不断得到补充。总反应如下:
业装置由200多个汞电解槽串联组成,每一个电解槽大小为15 m×2 m×0.3 m。这一工艺过程在 很高的电压下进行,消耗巨大的电能,合每吨氯气耗电3 MWh。由于该法存在一些缺点:汞很昂贵而且有毒,在汞循环时总有一些泄漏,与盐水反应生成氯化汞(II),因此该法仅生产一部分工业用氯气和氢氧化钠。
过去,这种工艺的废液排入湖泊和河流。鱼摄入 了汞化合物但无法排出,导致汞在鱼体内富集,达到很高的含量。现在,用过的盐水排放前要经过处理,将汞以硫化汞形式沉淀出来。近年来,改用另外两种不 用汞的电解槽生产大量需求的氯气和氢氧化钠:薄膜 电解槽和隔膜电解槽。在英国,使用的隔膜电解槽与汞电解槽的比例为1比20。在美国,隔膜电解槽与汞电解槽的比例为2比1。
2. 隔膜电解槽
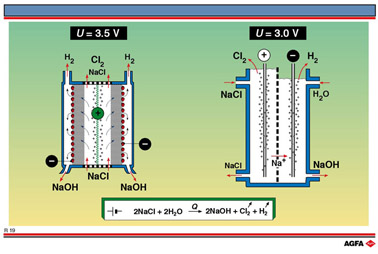
图 R19 左边部分说明隔膜电解槽。NaOH 和H2在带负电荷的阴极表面直接生成,Cl2在阳极生成。为了将氯气与氢氧化钠分开,传统上用多孔的石棉隔膜把两个半电池隔开,石棉隔膜需要每两个月更新一次。由于需要处理大量的石棉,该工艺对环境有害。幸运的是,现在能用聚合物替代部分石棉,制成的隔膜寿命长得多,不再需要如此频繁的更换。阳极用钛-钢合金制作,阴极用钢制成。电解前必须先除去盐水中的钙离子和镁离子杂质,否则它们会以不溶性氢氧化物形式沉淀出来,堵塞隔膜的孔隙。为了确保盐水通过隔膜从阳极流向阴极,保持阳极隔室的水位稍高一些。目前,在三种电解槽中,隔膜电解槽的技术最先进,有着非常出色的电化学性能。
3. 薄膜电解槽
图R19右边表示一种薄膜电解槽。它与隔膜槽非常相似,发生的反应也一样。主要的差别在于,在此 两个电极是用一层离子选择性聚合物膜分隔开。这种膜代替了石棉隔膜,只允许阳离子穿越。盐水从阳极 隔室的顶部泵入,水由阴极隔室的顶部引入。
在带负电的阴极上,水中的氢离子还原成氢气。在带正电的阳极上,盐水中的Cl-被氧化成氯气。Na+携带着电荷穿越薄膜,进入阴极隔室,与过剩的OH-形成NaOH。氯离子不能穿过膜,因而氯不能进入阴 极隔室,不能与其中的氢氧化钠接触。氢氧化钠从电解槽底部取走。
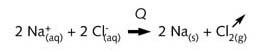
隔膜电解槽和薄膜电解槽中的总反应为:

与汞电解槽相比,两种隔膜电解槽的优点在于氯气和氢氧化钠不能接触。此外,它们耗电较少,因而运转花费较低。
参考文献
Buchner, Schliebs, Winter and Büchel, Industrial Inorganic Chemistry, VCH, Weinheim,
Germany.