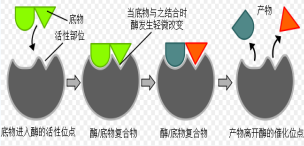
诱导契合模式详解图
酶的百科全书
----the Encyclopaedia of Enzyme
Chapter 2 酶的性质
诱导契合模式(Induced
fit)
该模式由丹尼尔・科什兰(Daniel Koshland)通过修改“锁-钥”模式,于1958年提出。基于的理论是,既然酶作为蛋白质,其结构是具有一定柔性的,因此活性位点在结合底物的过程中,通过与底物分子之间的相互作用,可以不断发生微小的形变。
在这一模式中,底物不是简单地结合到刚性的活性位点上,活性位点上的氨基酸残基的侧链可以摆动到正确的位置,使得酶能够进行催化反应。在结合过程中,活性位点不断地发生变化,直到底物完全结合,此时活性位点的形状和带电情况才会最终确定下来。在一些情况下,底物在进入活性中心时也是会发生微小形变的,如糖苷酶的催化反应。
Chapter 2 酶的性质

诱导契合模式详解图
1
.gif)